

Wirksamkeit
Die Wirksamkeit von Opzelura® wurde in zwei groß angelegten randomisierten Studien TRuE-V1 und TRuE-V2 untersucht. Mehr Informationen zum Studien-Design finden sie hier.
Im Folgenden finden Sie die Ergebnisse des Ansprechens gemäß dem Vitiligo Area Scoring Index (VASI).
NACH 52 WOCHEN: JEDER 2. PATIENT ERREICHTE UNTER OPZELURA® EINE 75%ige VERBESSERUNG DER FAZIALEN REPIGMENTIERUNG1
TRuE-V1: Der primäre Endpunkt, F-VASI75-Ansprechen in Woche 24, wurde von signifikant mehr Patienten unter Opzelura® als unter Vehikel erreicht.1,2
Nach 24 Wochen wurden Patienten unter Vehikel auf Opzelura® umgestellt.1
Ergebnisse des F-VASI75-Ansprechen waren in TRuE-V2 vergleichbar:
- Opzelura vs. Vehikel in Woche 24: 30,9% vs. 11,4%
- Opzelura vs. Vehikel inkl. Crossover in Woche 52: 48,0% vs. 29,6%
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung im Gesicht einher.1
Patient 1
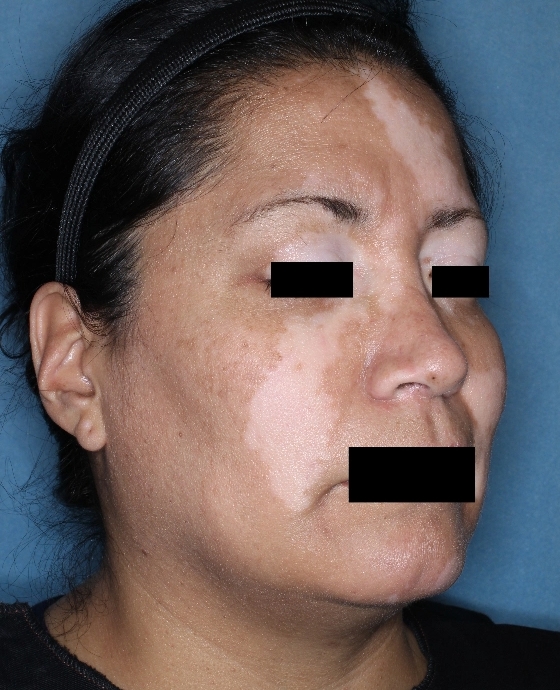
Woche 0
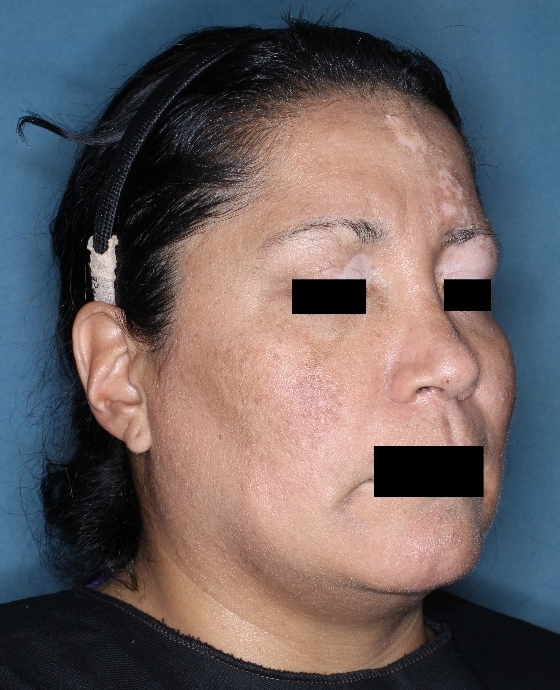
Woche 12
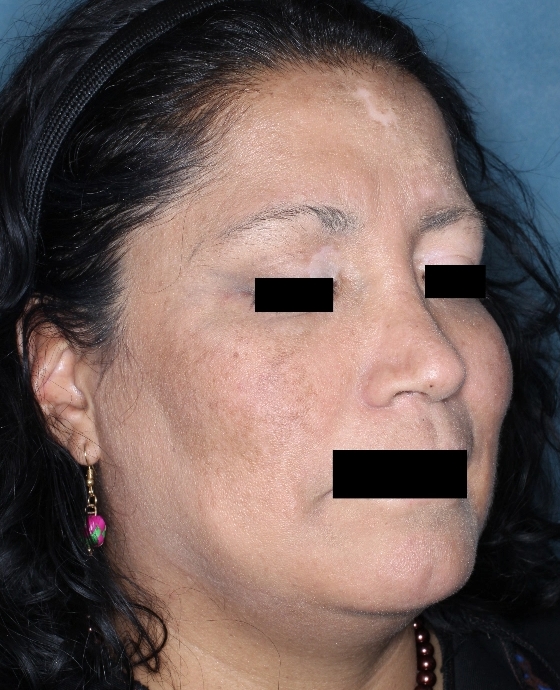
Woche 24
Patient 2

Woche 0
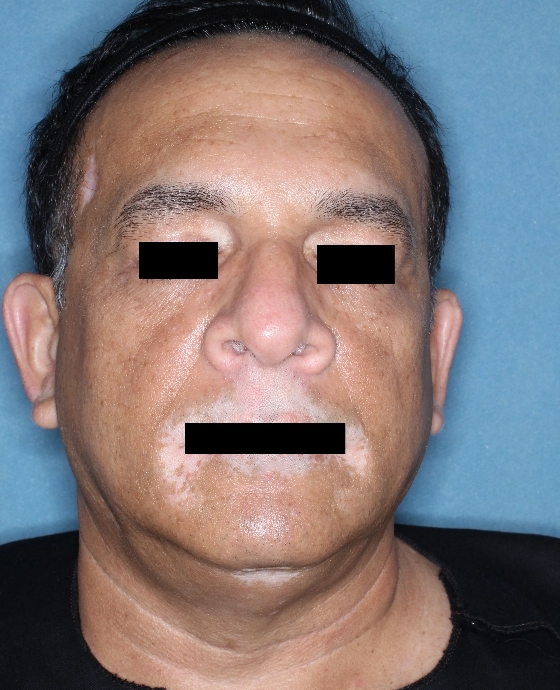
Woche 24
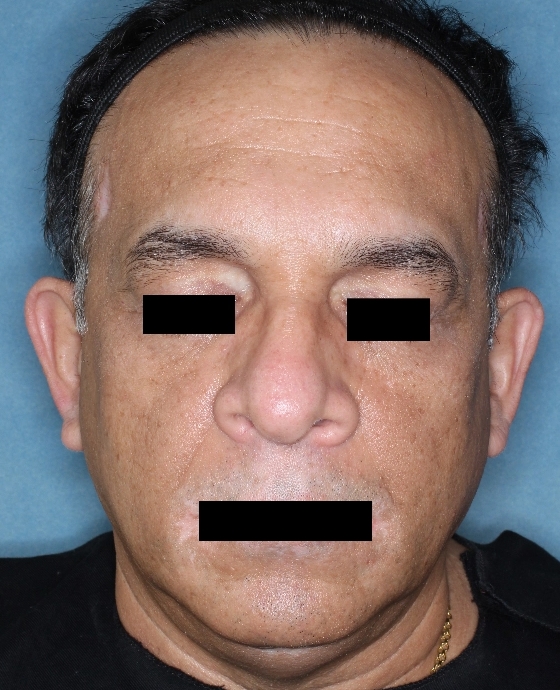
Woche 52
Patient 3
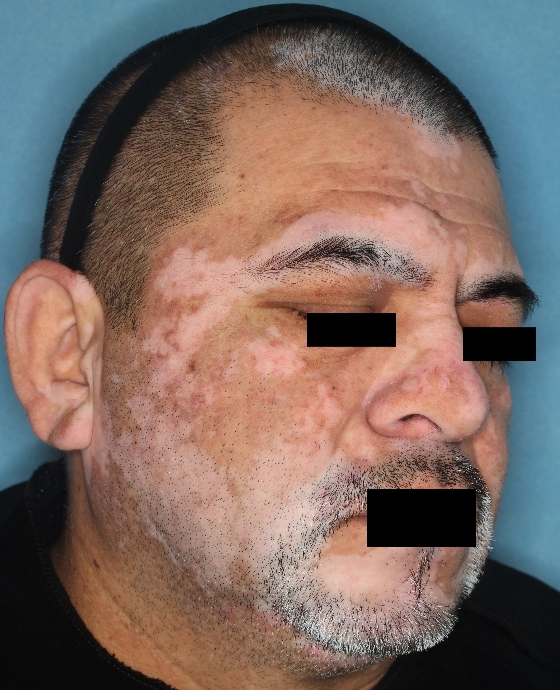
Woche 0
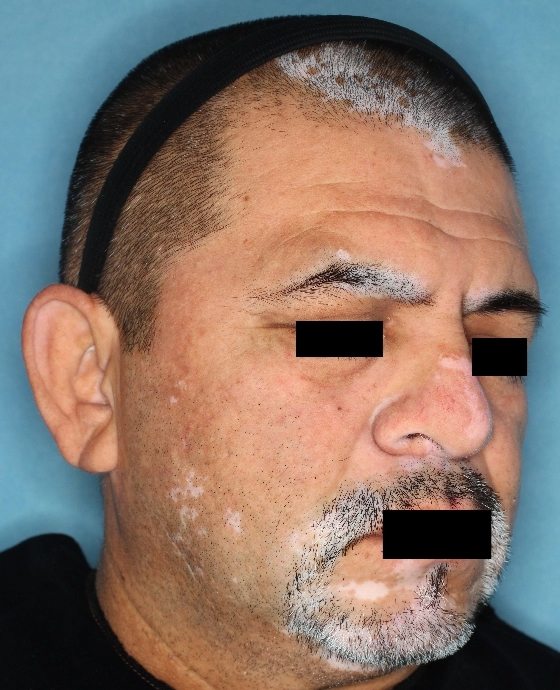
Woche 24
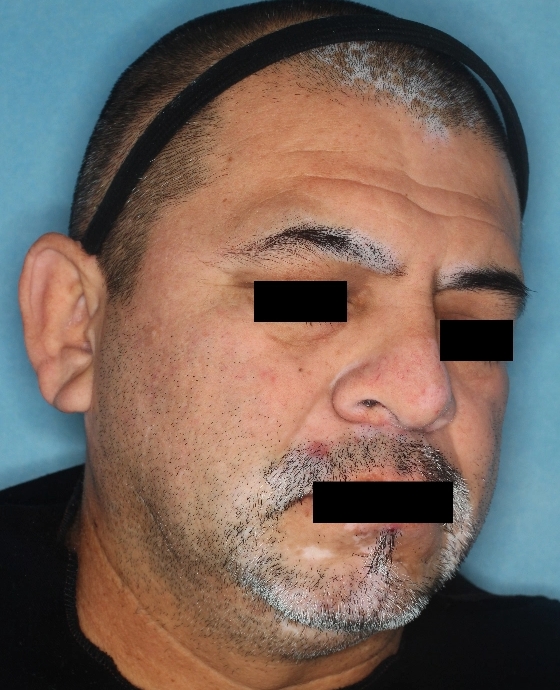
Woche 52
Patient 4
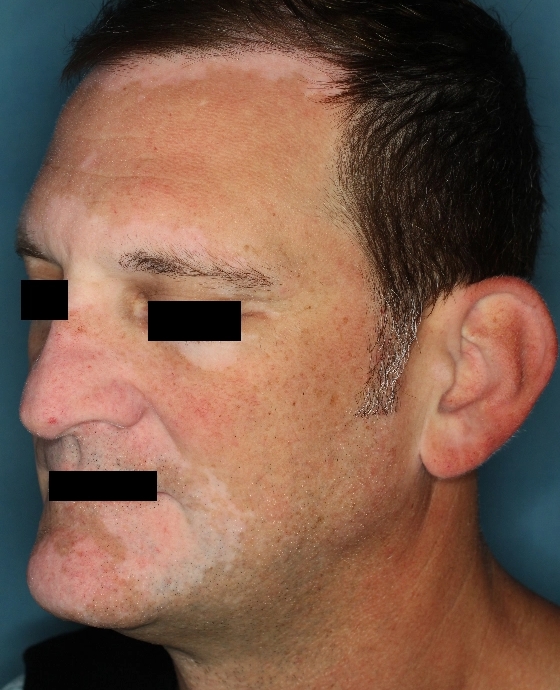
Woche 0
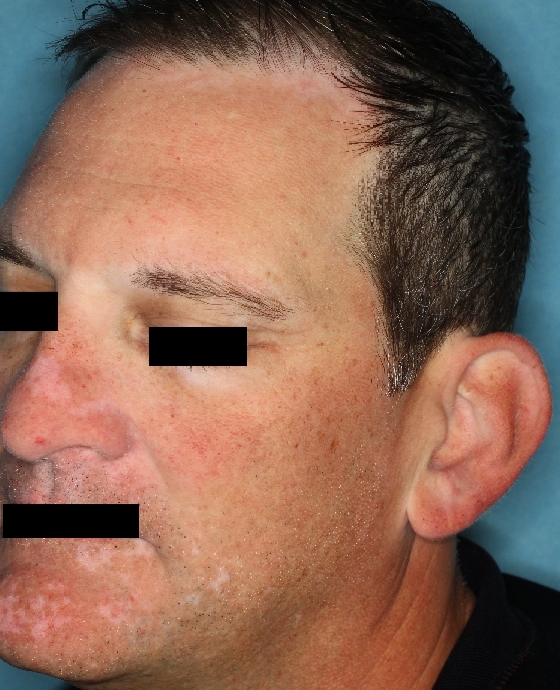
Woche 12
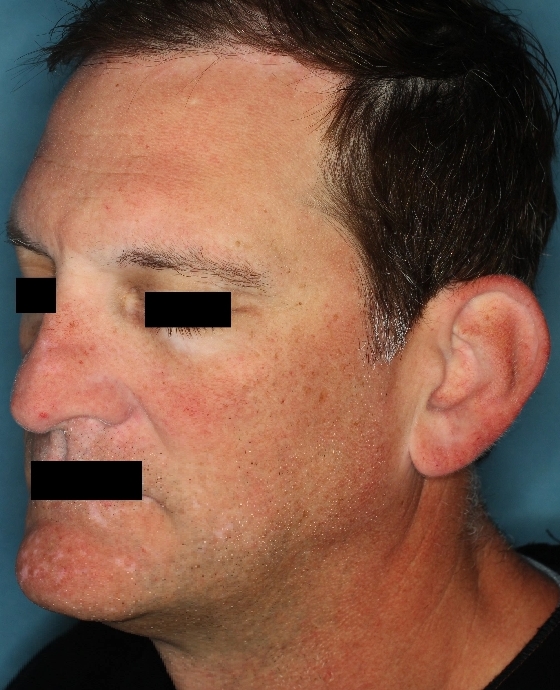
Woche 24
Patient 5

Woche 0

Woche 12

Woche 24
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung im Gesicht einher.1
Patient 1

Woche 0

Woche 12

Woche 24
Patient 2

Woche 0

Woche 24

Woche 52
Patient 3

Woche 0

Woche 24

Woche 52
Patient 4

Woche 0

Woche 12

Woche 24
Patient 5

Woche 0

Woche 12

Woche 24
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
NACH 12 WOCHEN: MEHR ALS 25 % DER PATIENTEN ZEIGTEN UNTER OPZELURA® EIN SCHNELLES F-FASI50-ANSPRECHEN1
TRuE-V1: ~ 3 von 4 Patienten erreichten mit Opzelura® eine ≥ 50 %ige Verbesserung der fazialen Repigmentierung gegenüber Baseline in Woche 52.*,1
Nach 24 Wochen wurden Patienten unter Vehikel auf Opzelura® umgestellt.1
Ergebnisse des F-VASI50-Ansprechen waren in TRuE-V2 vergleichbar:
- Opzelura vs. Vehikel in Woche 24: 51,4% vs. 20,9%
- Opzelura vs. Vehikel inkl. Crossover in Woche 52: 74,0% vs. 49,4%
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung im Gesicht einher.1
Patient 6

Woche 0
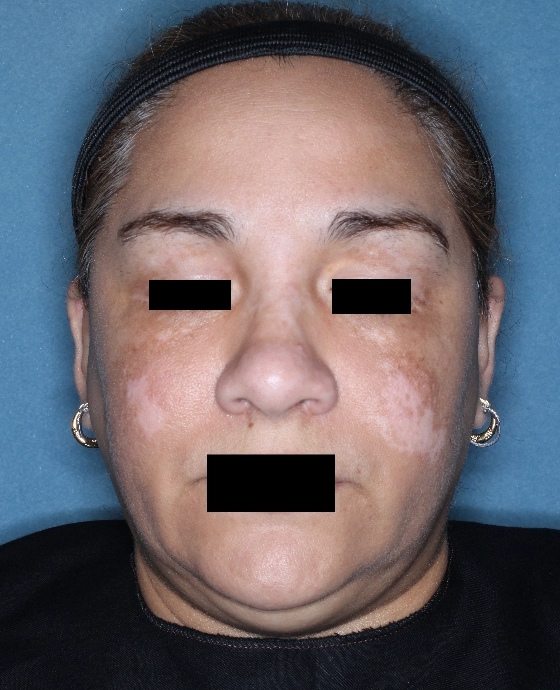
Woche 12
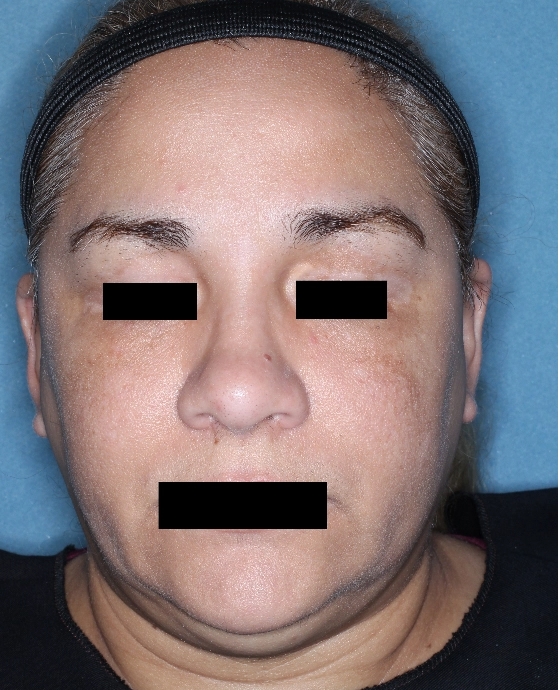
Woche 24
Patient 7
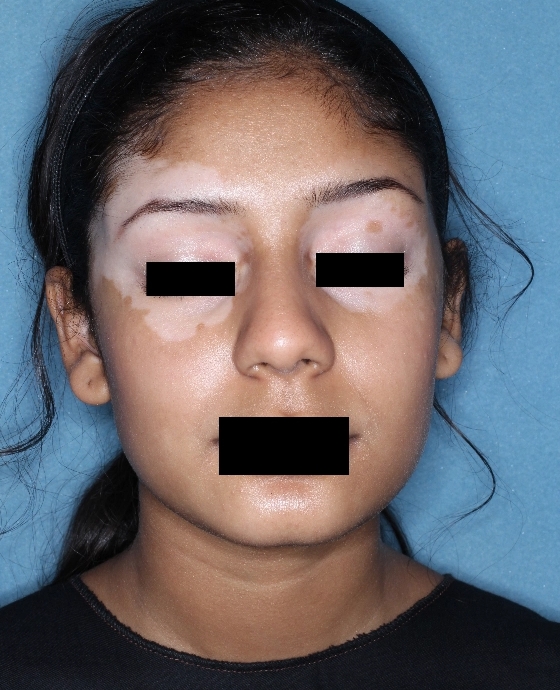
Woche 0
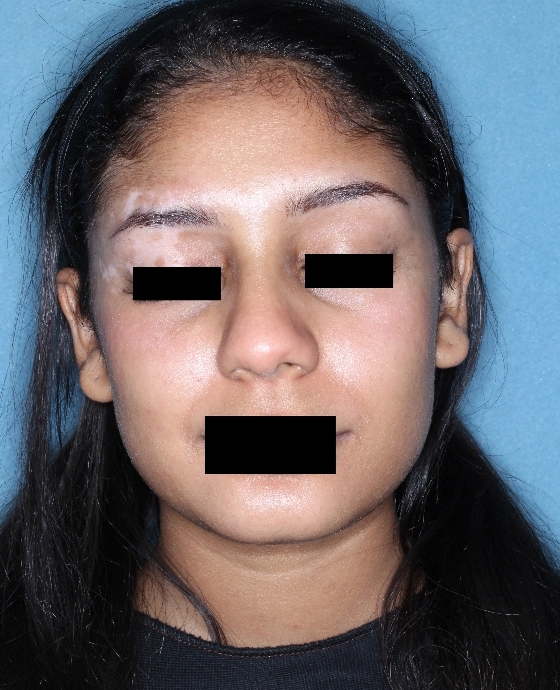
Woche 12
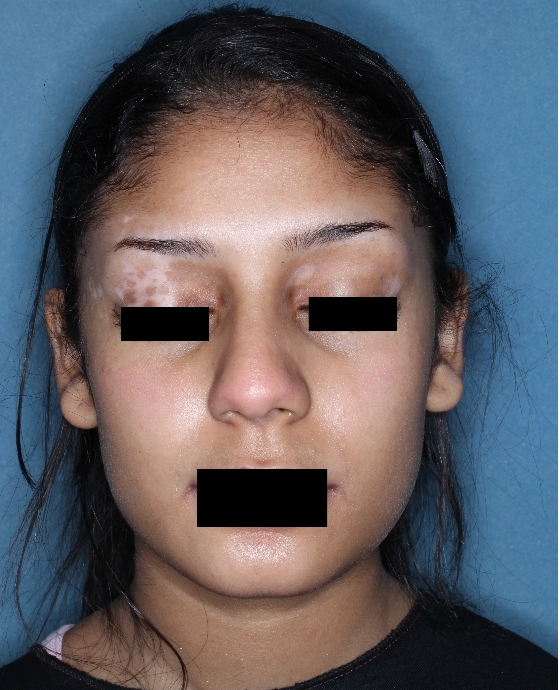
Woche 24
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung im Gesicht einher.1
Patient 6

Woche 0

Woche 12

Woche 24
Patient 7

Woche 0

Woche 12

Woche 24
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
NACH 1 JAHR: JEDER 3. PATIENT ERREICHTE ≥ 90 % FAZIALE REPIGMENTIERUNG UNTER OPZELURA1
F-VASI90-Ansprechen* in TRuE-V11
Ergebnisse des F-VASI90-Ansprechen waren in TRuE-V2 vergleichbar:
- Opzelura vs. Vehikel in Woche 24: 16,3% vs. 1,3%
- Opzelura vs. Vehikel inkl. Crossover in Woche 52: 27,7% vs. 16,0%
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung im Gesicht einher.1
Patient 8

Woche 0

Woche 24

Woche 52
Patient 9
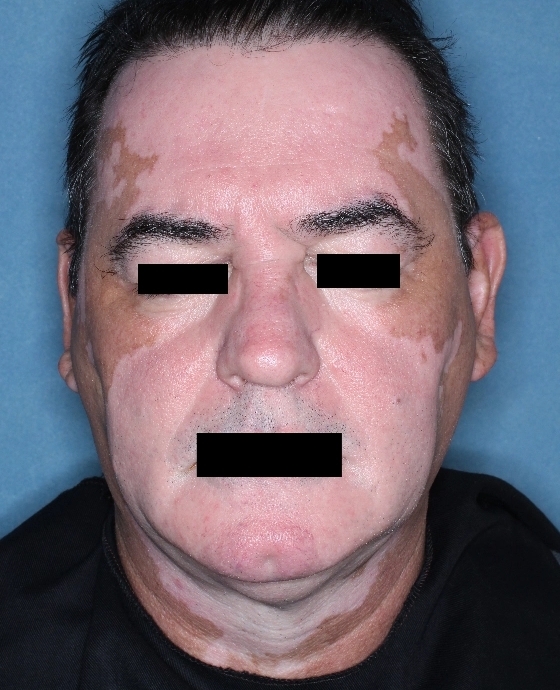
Woche 0
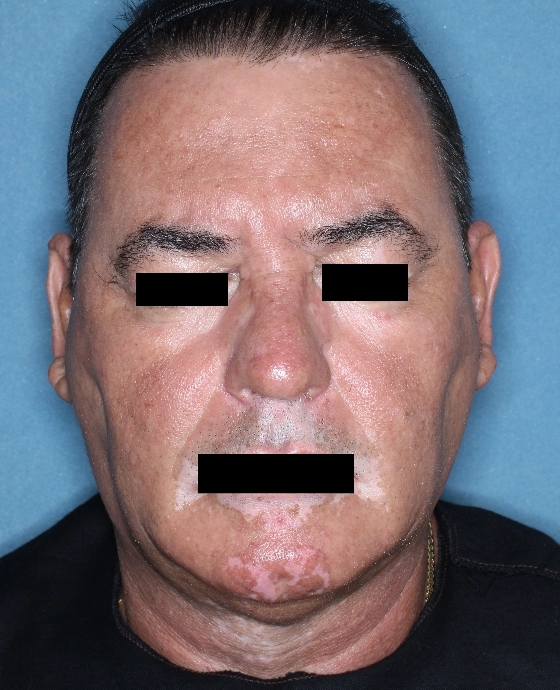
Woche 24
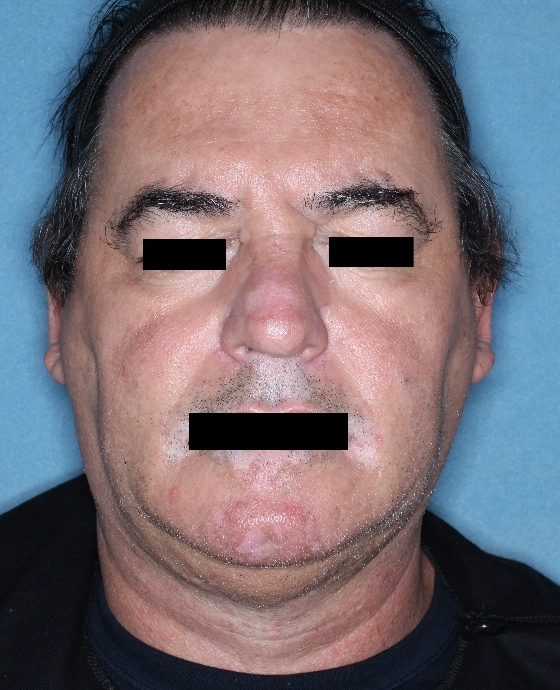
Woche 52
Patient 10
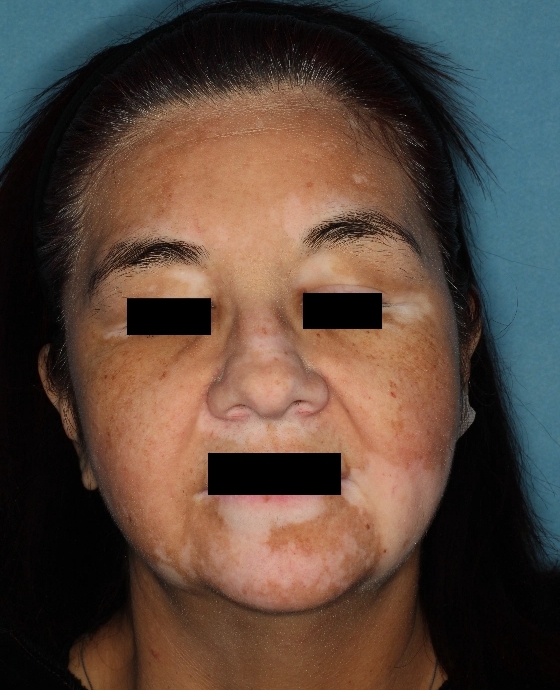
Woche 0
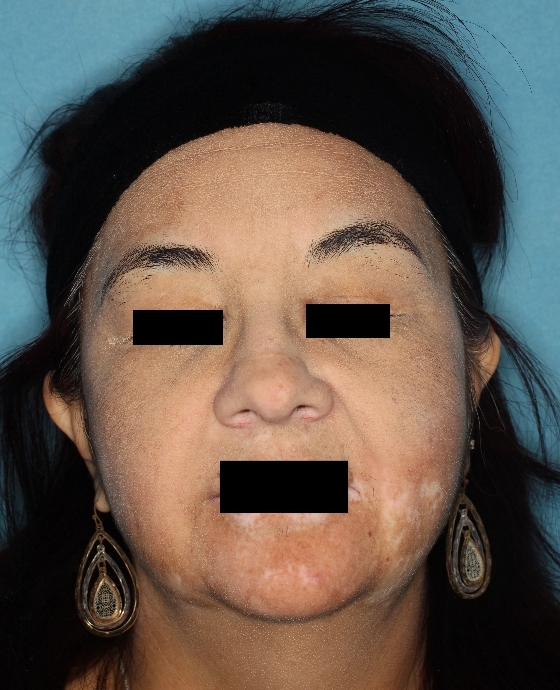
Woche 24

Woche 52
Patient 11
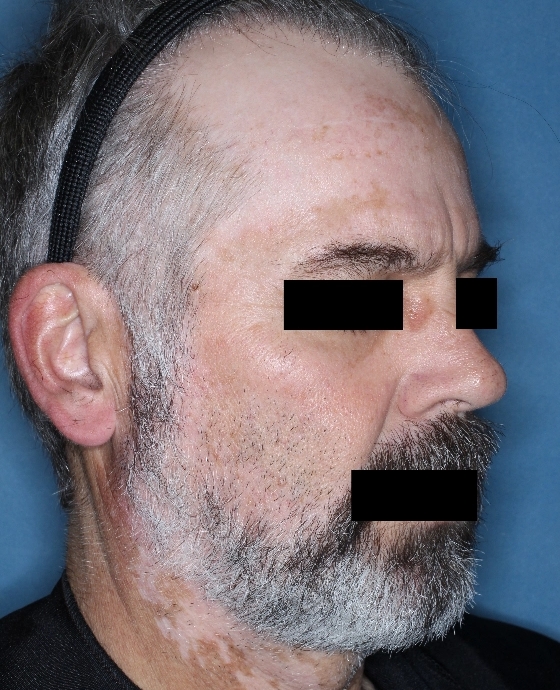
Woche 0
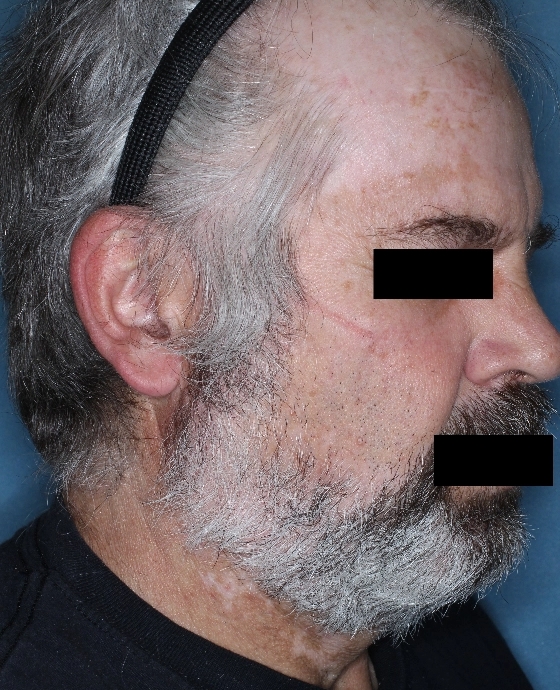
Woche 24
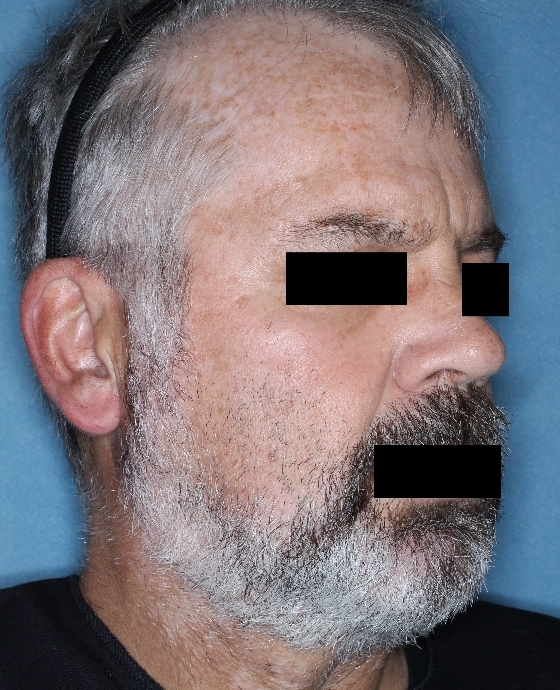
Woche 52
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung im Gesicht einher.1
Patient 8

Woche 0

Woche 24

Woche 52
Patient 9

Woche 0

Woche 24

Woche 52
Patient 10

Woche 0

Woche 24

Woche 52
Patient 11

Woche 0

Woche 24

Woche 52
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
NACH 1 JAHR: ~ JEDER 2. PATIENT ERREICHTE ≥ 50 % VERBESSERUNG DER GESAMTEN KÖRPERPIGMENTIERUNG1
Opzelura verbesserte signifikant die Repigmentierung im gesamten Körperbereich (T-VASI50) im Vergleich zu Vehikel.1
T-VASI50-Ansprechen* in TRuE-V11
Nach 24 Wochen wurden Patienten unter Vehikel auf Opzelura® umgestellt.1
Ergebnisse des T-VASI50-Ansprechen waren in TRuE-V2 vergleichbar:
- Opzelura vs. Vehikel in Woche 24: 23,9% vs. 6,8%
- Opzelura vs. Vehikel inkl. Crossover in Woche 52: 49,2% vs. 22,2%
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung am Körper einher.1
Patient 12
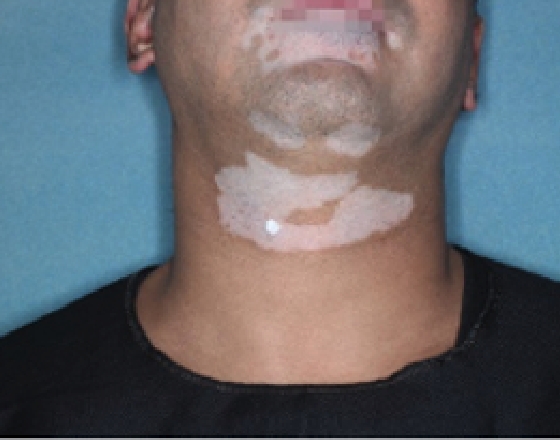
Baseline
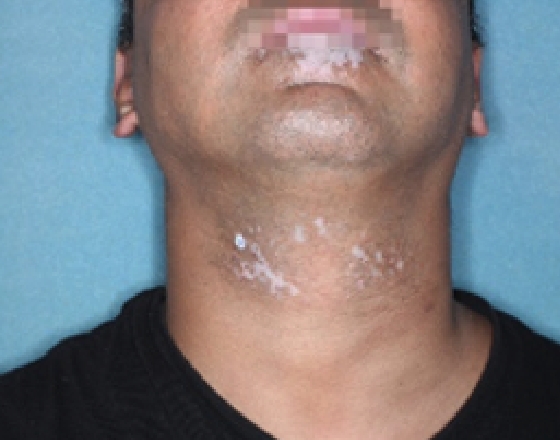
Woche 24

Woche 52
Patient 13
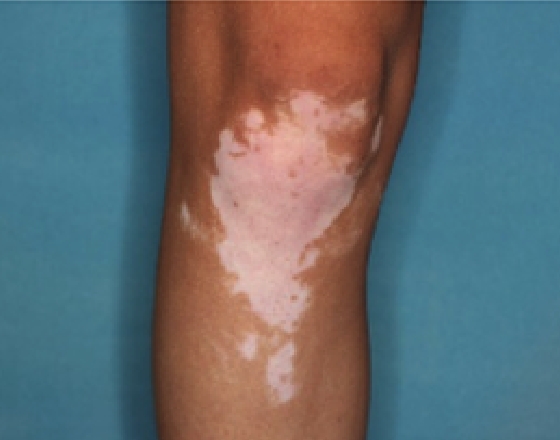
Baseline

Woche 24
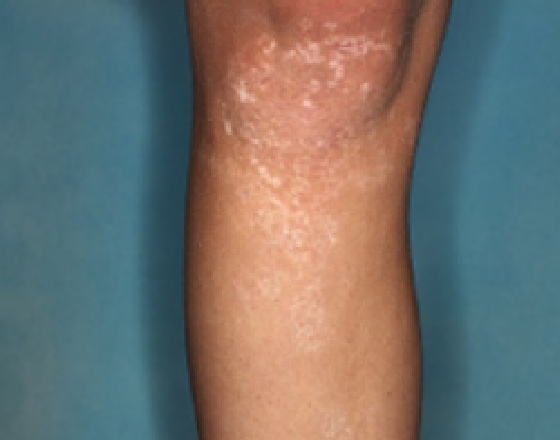
Woche 52
Patient 14
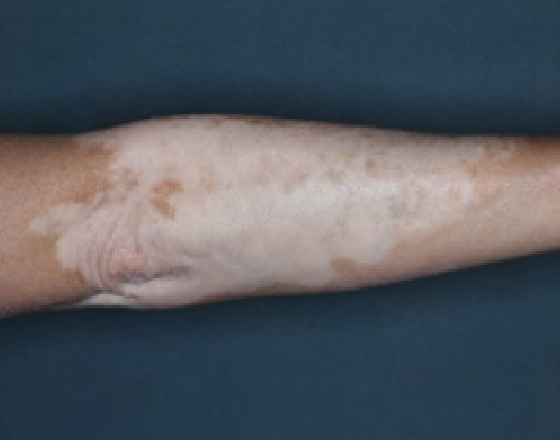
Baseline

Woche 24
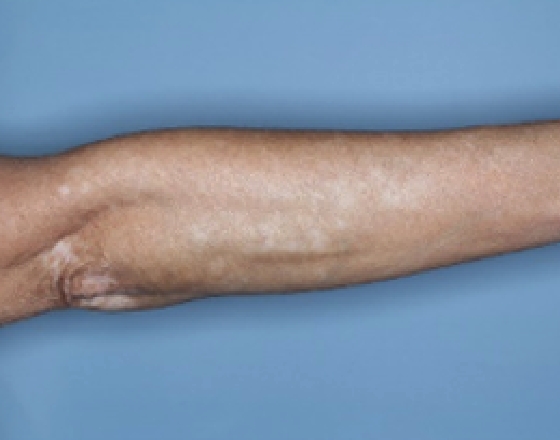
Woche 52
Patient 15
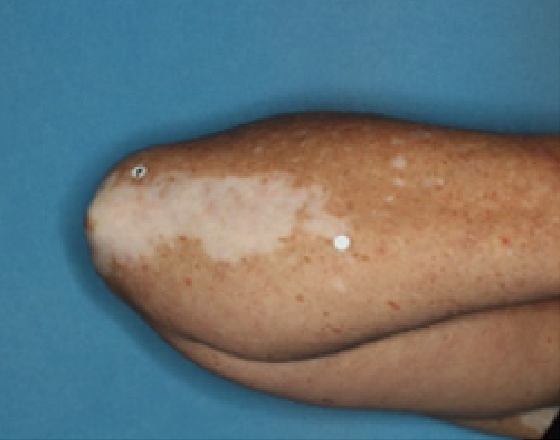
Baseline
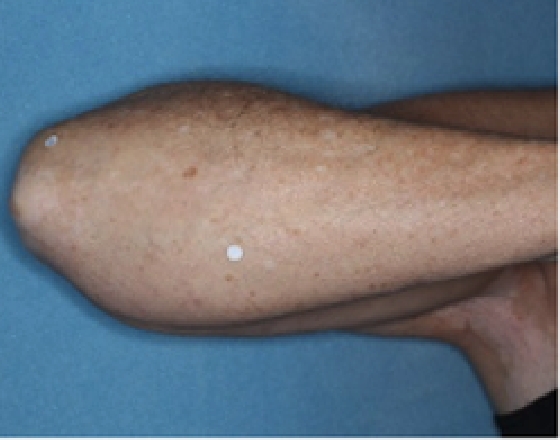
Woche 24
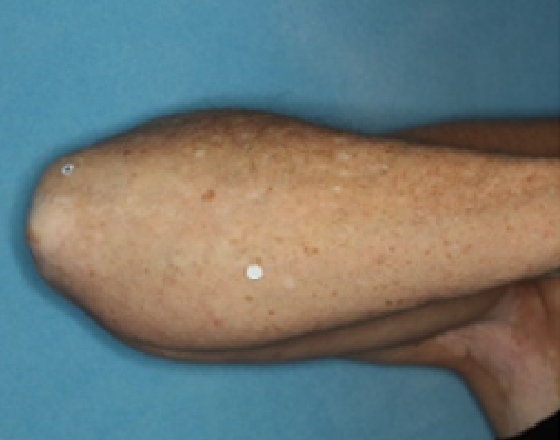
Woche 52
Patient 16
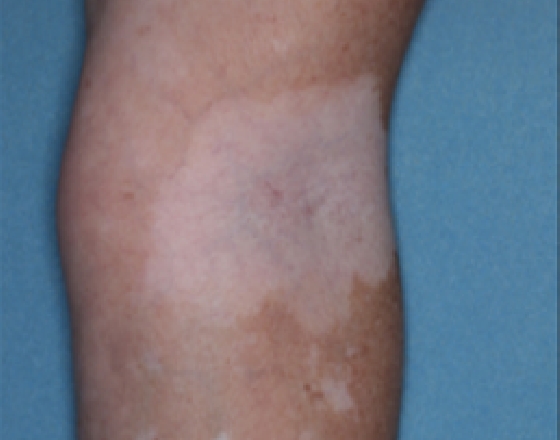
Baseline
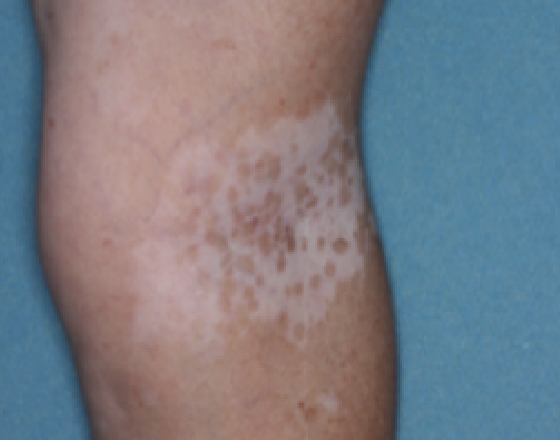
Woche 24
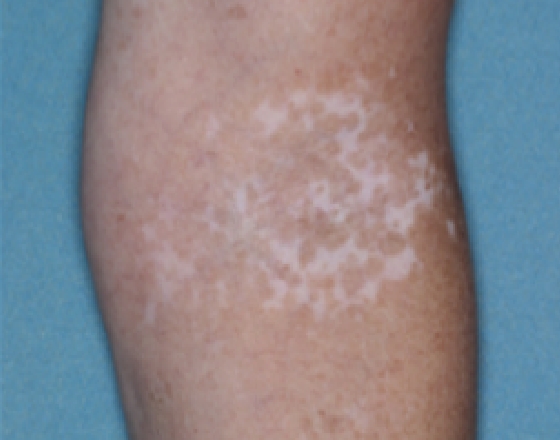
Woche 52
Patient 17
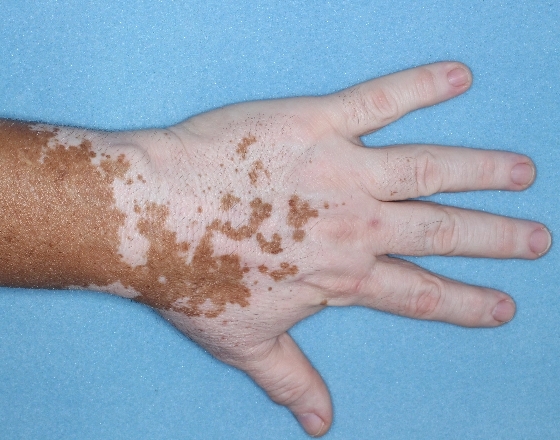
Baseline

Woche 24

Woche 52
Patient 18

Baseline

Woche 24

Woche 52
Patient 18 (Continued)
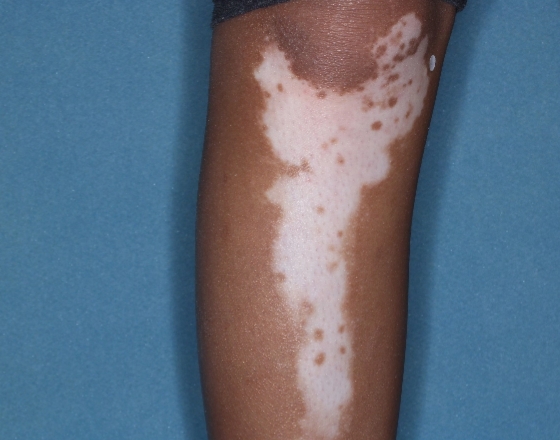
Baseline

Woche 24
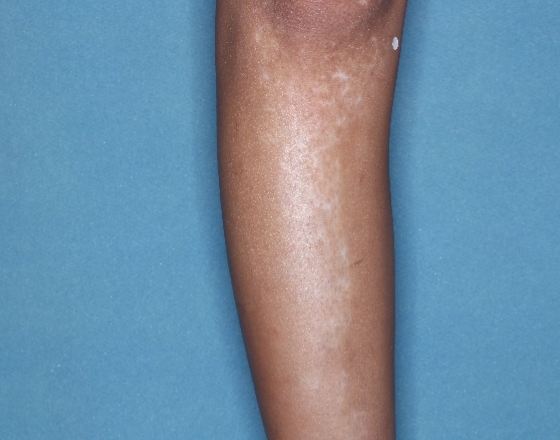
Woche 52
Patient 19

Baseline

Woche 24

Woche 52
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
Eine längere Behandlungszeit ging mit einer allmählichen und kontinuierlich zunehmenden Repigmentierung am Körper einher.1
Patient 12

Baseline

Woche 24

Woche 52
Patient 13

Baseline

Woche 24

Woche 52
Patient 14

Baseline

Woche 24

Woche 52
Patient 15

Baseline

Woche 24

Woche 52
Patient 16

Baseline

Woche 24

Woche 52
Patient 17

Baseline

Woche 24

Woche 52
Patient 18

Baseline

Woche 24

Woche 52
Patient 18 (Continued)

Baseline

Woche 24

Woche 52
Patient 19

Baseline

Woche 24

Woche 52
Die folgenden Abbildungen zeigen verschiedene Behandlungsverläufe mit Opzelura® aus den TruE-V-Zulassungsstudien über einen Zeitraum von bis zu einem Jahr. Der jeweils erreichte Repigmentierungsgrad kann im Behandlungsverlauf individuell variieren.
PATIENTEN BEWERTETEN IHRE VITILIGO ALS „WENIGER WAHRNEHMBAR“ DURCH DIE BEHANDLUNG MIT OPZELURA®
In der TRuE-V1 Zulassungsstudie erreichten in Woche 24 signifikant mehr Patienten, die mit Opzelura® behandelt wurden, ein VNS-Ansprechen (bewertet als „etwas weniger wahrnehmbar“ oder „nicht mehr wahrnehmbar“) im Vergleich zu Vehikel.1
VNS-Ansprechen: TRuE-V1 und TRuE-V2 zeigten vergleichbare Ergebnisse1
- Opzelura vs. Vehikel in Woche 24: 20,5% vs. 4,9%
- Opzelura vs. Vehikel inkl. Crossover in Woche 52: 32,8% vs. 13,6%
F-PaGIC-V, Facial Patient Global Impression of Change for Vitiligo; VNS, Vitiligo Noticeability Scale; TRuE-V, Topical Ruxolitinib Evaluation in Vitiligo study.
ZWEI GROSS ANGELEGTE RANDOMISIERTE STUDIEN UNTERSUCHTEN DIE WIRKSAMKEIT VON OPZELURA®1,3
VASI, Vitiligo Area Scoring Index; F-VASI, faziale Vitiligo Area Scoring Index; TEAE, therapie-assoziiertes unerwünschtes Ereignis; VNS, Vitiligo Noticeability Scale-Score bid, 2x täglich.
Primärer Endpunkt1,3
- F-VASI75: Anteil der Patienten mit einer 75%igen Verbesserung des F-VASI gegenüber Baseline in Woche 24
Sekundäre Endpunkte1,4
- F-VASI50: Anteil der Patienten mit einer 50%igen Verbesserung des F-VASI gegenüber Baseline in Woche 24 und 52
- F-VASI90: Anteil der Patienten mit einer 90%igen Verbesserung des F-VASI gegenüber Baseline in Woche 24 und 52
- Anteil der Patienten mit einer signifikanten Reduktion des VNS
- Therapie-assoziierte unerwünschte Ereignisse (TEAE)
VASI, Vitiligo Area Scoring Index; F-VASI, faziale Vitiligo Area Scoring Index; TEAE, therapie-assoziiertes unerwünschtes Ereignis; VNS, Vitiligo Noticeability Scale-Score.
DIE BASELINE CHARAKTERISTIK DER STUDIENPOPULATION
WAREN IN TRUE-V1 UND TRUE-V2 ÄHNLICH VERTEILT.
Baseline Charakteristika in TRuE-V11
Baseline Charakteristika waren in TRuE-V1 und TRuE-V2 ähnlich verteilt1
*Der Wert berechnet sich aus folgenden Einzelkomponenten: NB-UVB Phototherapie, Excimer-Lasertherapie und PUVA Photochemotherapie. Total body surface area; TCI, Topische Kalzineurininhibitoren; TCS, Topische Kortikosteroide; TRuE-V, Topical Ruxolitinib Evaluation in Vitiligo study
- 1. Rosmarin D, Passeron T, Pandya AG, et al. Two Phase 3, randomized, controlled trials of ruxolitinib cream for vitiligo. N Engl J Med. 2022;387(16):1445-1455.
- 2. Incyte Biosciences International Sarl. Data on File.
- 3. Rosmarin D. Efficacy and safety of ruxolitinib crem monotherapy for the treatment of vitiligo: results from 2 52-week phase 3 studies. #S026. Presented at: AAD 2022 Annual Meeting; 25–29 March; Boston, MA, USA.
- 4. Bibeau K, Parsad D, Harris J, et al. Exploring the Natural and Treatment History of Vitiligo: Findings From the Global VALIANT Study. Presented at: Maui Derm for Dermatologists; January 24, 2022; Grand Wailea, Maui, HI.
- 5. Batchelor JM, Tan W, Tour S, Yong A, Montgomery AA, Thomas KS. Validation of the Vitiligo Noticeability Scale: a patient-reported outcome measure of vitiligo treatment success. Br J Dermatol. 2016;174(2):386-394.
- 6. Passeron T. Medical and Maintenance Treatments for Vitiligo. Dermatol Clin. 2017;35(2):163-170.
VNS5
Der Erfolg einer Behandlung kann über die Vitiligo Noticeability Scale (VNS) gemessen werden. Einem Beurteilungssystem, das von Patienten dokumentiert wird und anhand einer 5-Punkte-Skala erfolgt.
Die Patienten wurden gebeten, Fotos von Vitiligo vor und nach der Behandlung zu vergleichen und die Auffälligkeit wie folgt zu bewerten:
- Stärker auffällig
- Genauso auffällig
- Geringfügig weniger auffällig
- Viel weniger auffällig
- Nicht mehr auffällig
Ein Ergebnis von 4 oder 5 wurde als Reaktion gewertet. Die VNS wurde für Vitiligo-Läsionen im Gesicht evaluiert.
F-PaGIC-V6
Mit Hilfe des Facial Patient Global Impression of Change for Vitiligo (F-PaGIC-V) – einer 7-Punkte-Skala – kann der Patient selbst bewerten, wie sich seine Vitiligo verbessert hat.1
Nach 24 Wochen berichteten signifikant mehr Opzelura-Patienten von einer Verbesserung gemäß F-PaGIC-V („sehr stark verbessert“ oder „stark verbessert“) im Vergleich zur Vehikel-Gruppe (45,1 % vs. 7,8 %; p < 0,0001).1
Colour matching6
Über eine 5-stufige Skala wird das Colour matching erfasst: „Ausgezeichnet“, „Sehr gut“, „Gut“, „Schlecht“ and „Sehr schlecht“.1
Nach 24 Wochen berichteten signifikant mehr Opzelura-Patienten von einem „guten“ oder besseren Colour matching im Vergleich zur Vehikel-Gruppe (76,9 % gegenüber 43,3 %; p < 0,0001).1
Berechnung des VASI*
Fläche der Vitiligo-Läsionen X Grad der Depigmentierung innerhalb der Läsionen

100%

90%

75%

50%
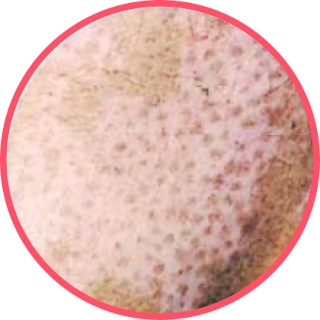
25%

10%
VASI, Vitiligo Area Scoring Index
*Data on file.1
Patient characteristics from TRuE-V134
| Additional baseline characteristics for TRuE-V1 | ||
|---|---|---|
| Vehicle cream (n=109) | Opzelura (n=221) | |
| Race or ethnic group, n (%)* | ||
| White | 96 (88.1) | 180 (81.4) |
| Black | 4 (3.7) | 11 (5.0) |
| Asian | 4 (3.7) | 5 (2.3) |
| Other | 2 (1.8) | 9 (4.1) |
| Not reported | 3 (2.8) | 16 (7.2) |
| Geographic region, n (%) | ||
| North America | 73 (67.0) | 147 (66.5) |
| Europe | 36 (33.0) | 74 (33.5) |
| F-VASI, mean±SD† | 1.0±0.6 | 0.9±0.6 |
| T-VASI, mean±SD‡ | 6.4±1.9 | 6.5±2.0 |
| Facial BSA affected by vitiligo, %§ | 1.2±0.7 | 1.05±0.7 |
| Total BSA affected by vitiligo, % | 7.2±2.0 | 7.3±2.0 |
| Received diagnosis in childhood, n (%) | 34 (31.2) | 72 (32.6) |
| Other autoimmune disorders, n (%)¶ | 18 (16.5) | 53 (24.0) |
| Thyroid disorders | 17 (15.6) | 50 (22.6) |
| Additional baseline characteristics for TRuE-V1 | ||||
|---|---|---|---|---|
| Vehicle cream (n=109) | Opzelura (n=221) | |||
| Juvenile diabetes mellitus | 1 (0.9) | 0 | ||
| Pernicious anaemia | 0 | 1 (0.5) | ||
| Other | 1 (0.9) | 5 (2.3) | ||
| Previous therapy, n (%)** | 61 (56.0) | 131 (59.3) | ||
| Topical calcineurin inhibitors | 31 (28.4) | 72 (32.6) | ||
| Topical glucocorticoids | 28 (25.7) | 67 (30.3) | ||
| NB-UVB phototherapy | 20 (18.3) | 41 (18.6) | ||
| Excimer laser therapy | 8 (7.3) | 18 (8.1) | ||
| PUVA photochemotherapy | 4 (3.7) | 8 (3.6) | ||
| Vitamin D derivatives | 2 (1.8) | 4 (1.8) | ||
| Other | 11 (10.1) | 24 (10.9) | ||
* Race and ethnic group were reported by the patient. “Other” includes American Indian or Alaska Native, Native Hawaiian or Pacific Islander, and other.
† Scores on the F-VASI range from 0 to 3, with higher scores indicating a greater area of facial depigmentation.
‡ Scores on the T-VASI range from 0 to 100, with higher scores indicating a greater area of total body depigmentation.
§ Shown is the percentage of total BSA.
¶ Patients could report multiple autoimmune disorders.
** Patients could have used multiple previous lines of therapy. “Other” includes other types of phototherapy, oral glucocorticoids, surgical techniques, and other.
BSA, body surface area; F-VASI, Facial Vitiligo Area Scoring Index; NB-UVB, narrowband ultraviolet B; PUVA, psoralen ultraviolet A; SD, standard deviation; T-VASI, Total Vitiligo Area Scoring Index.
Baseline characteristics in TRuE-V2 were similar to TRuE-V134
| Baseline characteristics for TRuE-V2 | ||
|---|---|---|
| Vehicle cream (n=115) | Opzelura (n=228) | |
| Age (years) mean±SD | 39.8±12.1 | 38.4±15.2 |
| Age group, n (%) | ||
| 12–17 | 6 (5.2) | 30 (13.2) |
| 18–64 | 106 (92.2) | 186 (81.6) |
| ≥65 | 3 (2.6) | 12 (5.3) |
| Female sex, n (%) | 60 (52.2) | 112 (49.1) |
| Race or ethnic group, n (%)* | ||
| White | 93 (80.9) | 182 (79.8) |
| Black | 5 (4.3) | 12 (5.3) |
| Asian | 7 (6.1) | 12 (5.3) |
| Other | 7 (6.1) | 19 (8.3) |
| Not reported | 3 (2.6) | 3 (1.3) |
| Fitzpatrick skin type, n (%)† | ||
| Baseline characteristics for TRuE-V2 | ||||
|---|---|---|---|---|
| Vehicle cream (n=115) | Opzelura (n=228) | |||
| I | 1 (0.9) | 2 (0.9) | ||
| II | 32 (27.8) | 57 (25.0) | ||
| III | 45 (39.1) | 89 (39.0) | ||
| IV | 25 (21.7) | 55 (24.1) | ||
| V | 10 (8.7) | 17 (7.5) | ||
| VI | 2 (1.7) | 8 (3.5) | ||
| Geographic region, n (%) | ||||
| North America | 83 (72.2) | 160 (70.2) | ||
| Europe | 32 (27.8) | 68 (29.8) | ||
| F-VASI, mean±SD‡ | 0.8±0.5 | 0.9±0.5 | ||
| T-VASI, mean±SD§ | 7.0±2.2 | 6.8±2.1 | ||
| Facial BSA affected by vitiligo, %¶ | 0.9±0.6 | 1.0±0.56 | ||
| Total BSA affected by vitiligo, % | 7.7±2.0 | 7.4±2.0 | ||
| Duration of disease (years) | 16.0±11.6 | 15.9±12.1 | ||
| Baseline characteristics for TRuE-V2 | ||||
|---|---|---|---|---|
| Vehicle cream (n=115) | Opzelura (n=228) | |||
| Received diagnosis in childhood, n (%) | 43 (37.4) | 96 (42.1) | ||
| Disease stability, n (%)** | ||||
| Stable | 88 (76.5) | 166 (72.8) | ||
| Progressive | 27 (23.5) | 62 (27.2) | ||
| Other autoimmune disorders, n (%)†† | 18 (15.7) | 37 (16.2) | ||
| Thyroid disorders | 15 (13.0) | 35 (15.4) | ||
| Juvenile diabetes mellitus | 0 | 0 | ||
| Pernicious anaemia | 0 | 0 | ||
| Other | 6 (5.2) | 5 (2.2) | ||
| Previous therapy, n (%)‡‡ | 76 (66.1) | 143 (62.7) | ||
| Topical calcineurin inhibitors | 37 (32.2) | 74 (32.5) | ||
| Topical glucocorticoids | 28 (24.3) | 66 (28.9) | ||
| NB-UVB phototherapy | 27 (23.5) | 52 (22.8) | ||
| Baseline characteristics for TRuE-V2 | ||||
|---|---|---|---|---|
| Vehicle cream (n=115) | Opzelura (n=228) | |||
| Excimer laser therapy | 14 (12.2) | 16 (7.0) | ||
| PUVA photochemotherapy | 8 (7.0) | 15 (6.6) | ||
| Vitamin D derivatives | 1 (0.9) | 0 | ||
| Other | 14 (12.2) | 34 (14.9) | ||
* Race and ethnic group were reported by the patient. “Other” includes American Indian or Alaska Native, Native Hawaiian or Pacific Islander, and other.
† Fitzpatrick skin types range from I to VI: type I indicates pale white; type II, white; type III, light brown; type IV, moderate brown; type V, dark brown; and type VI, deeply pigmented dark brown to black.
‡ Scores on the F-VASI range from 0 to 3, with higher scores indicating a greater area of facial depigmentation.
§ Scores on the T-VASI range from 0 to 100, with higher scores indicating a greater area of total body depigmentation.
¶Shown is the percentage of total BSA.
**The determination of disease stability was based on investigator judgment.
††Patients could report multiple autoimmune disorders.
‡‡ Patients could have used multiple previous lines of therapy. “Other” includes other types of phototherapy, oral glucocorticoids, surgical techniques, and other.
BSA, body surface area; F-VASI, Facial Vitiligo Area Scoring Index; NB-UVB, narrowband ultraviolet B; PUVA, psoralen ultraviolet A; SD, standard deviation; T-VASI, Total Vitiligo Area Scoring Index.
